¿Qué es la enfermedad de BATTEN (CLN6)?
Las personas con enfermedad de Batten nacen sanas y alcanzan los hitos de desarrollo esperados en los primeros años de edad, pero con el tiempo, revierten progresivamente sus logros de desarrollo, perdiendo gradualmente sus capacidades intelectuales, motoras, visuales y pueden desarrollar epilepsia y trastornos del movimiento.
Los tipos principales de enfermedad de Batten se clasifican en la actualidad en función de los defectos genéticos específicos que afectan distintos niveles dentro de las células. Así, hay 14 subtipos en total, desde la CLN1 que se descubrió en 1995, hasta la CLN14 (2012). Las distintas formas de NCL tienen muchos síntomas y signos comunes, como crisis epilépticas, deterioro psicomotor progresivo y déficit visual. Varían en edad de inicio y gravedad, desde la etapa de recién nacido hasta la edad adulta, y esa variedad es debida a distintos factores genéticos, como la herencia y el tipo de mutación que portan (lo que se llama correlación genotipo-fenotipo).
La herencia es habitualmente autosómica recesiva, es decir, cada progenitor es portador y en cada embarazo de esa pareja el riesgo de transmisión de la enfermedad es del 25%. El gen que está alterado es diferente en cada tipo de NCL y dentro de cada gen puede haber
muy distintos tipos de mutaciones. Así, en dos familias con hijos o hijas con el mismo tipo de NCL (por ejemplo, CLN6), pueden presentar mutaciones diferentes en ese mismo gen (hay más de 70 diferentes para CLN6, por ejemplo).
Desde el punto de vista de edad de inicio de síntomas, las NCL se pueden clasificar en:
– NCL infantil tardía, que comienza entre los 3 y los 8 años. Por lo general, los pacientes viven entre 8 y 12 años. En este grupo está la que padecen Hodei e Ilargi, la CLN6.
– NCL juvenil, que comienza entre los 5 y los 8 años de edad. Muchos de estos pacientes viven hasta la adolescencia o hasta los 20 años.
– NCL adulta, que comienza antes de los 40 años de edad. Los pacientes pueden llegar a tener una expectativa de vida normal.
Síntomas
- Retraso intelectual y del desarrollo.
- Cambios en la personalidad y el comportamiento.
- Demencia o confusión.
- Crisis epilépticas de tipo mioclonias, caídas o convulsiones
- Pérdida de la visión.
- Alteraciones del sueño.
- Contracciones musculares involuntarias.
- Ataxia o inestabilidad para caminar o mantenerse de pie.
- Pérdida de la capacidad para caminar, hablar o comunicarse.
En el caso de Hodei, la enfermedad le afectó desde un principio en el desarrollo del lenguaje. No ha llegado a hablar, y las pocas palabras que decía las fue perdiendo. También le ha ido afectando en la movilidad y en la visión. Pasó de ser un niño con muy buena motricidad, capaz de correr, saltar, nadar… a tener problemas para caminar o sostenerse por sí mismo.
Ilargi inició con síntomas entre los 4 y los 6 años, también con afectación a nivel motriz y con retroceso en el desarrollo del lenguaje. Sin embargo, gracias al tratamiento con Miglustat el avance de los síntomas ha sido más lento que en Hodei, llegando incluso a recuperar en algunas áreas.
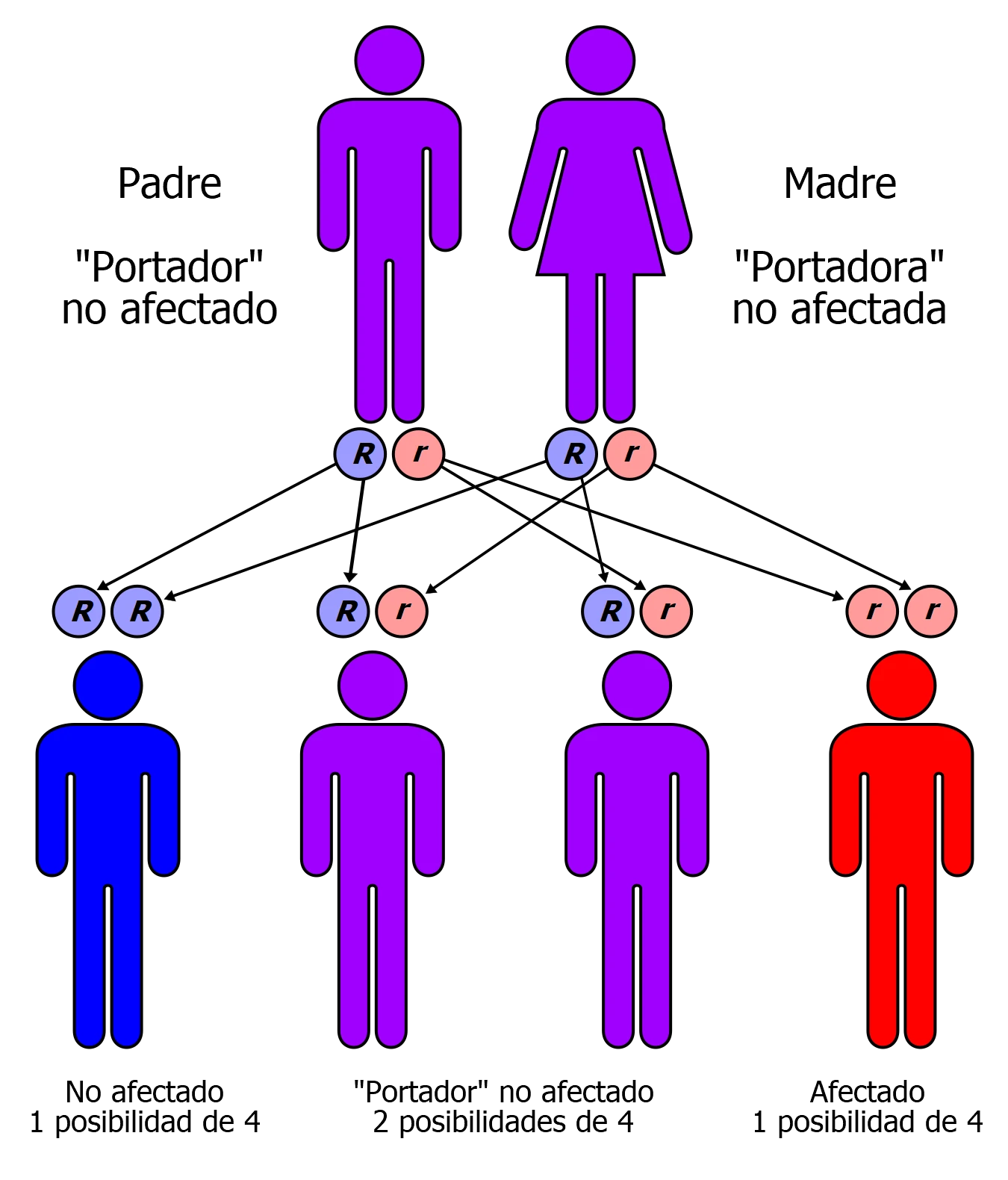
Esta enfermedad es un trastorno autosómico recesivo. Esto significa que cuando ambos progenitores son portadores de cada una de las dos copias del gen defectuoso que genera la enfermedad, tienen una posibilidad de entre cuatro (25%) de transmitirlo a cada uno de sus hijos o hijas.
Sin tratamientos aprobados, la enfermedad CLN6 de Batten es una enfermedad neurológica mortal que priva rápidamente a los niños y niñas de su capacidad para caminar, hablar, pensar y ver.
Hasta la actualidad, el único tratamiento que existe, con potencial de ser un modificador del curso de la enfermedad, es una terapia génica inicialmente desarrollada por Amicus Therapeutics y con un primer ensayo clínico llevado a cabo en el Nationwide Children’s Hospital en Columbus, Ohio, en el que participaron 13 pacientes.
Actualmente, está previsto lanzar un segundo ensayo clínico, impulsado por la Fundación Cure Batten y esta vez de la mano del Children’s Hospital of Orange County (CHOC) en California.
Este tratamiento actualmente en estudio consiste en reemplazar el gen mutado del paciente de Batten CLN6 mediante la entrega de un nuevo gen que es transportado al cerebro por un virus que no es dañino para los humanos.
Adicionalmente, se está trabajando en la aprobación de un tratamiento complementario para la enfermedad de Batten basado en el fármaco Miglustat. Este fármaco ya está aprobado para su uso con otras enfermedades, y se han observado efectos muy positivos en pacientes con enfermedad de Batten.
Información útil, estudios y publicaciones sobre la enfermedad de Batten
- Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares. Definicion, tratamientos, pronosticos y estudios clinicos de la enfermedad BATTEN
- Amicus Therapeutics. Amicus anuncia datos clínicos provisionales positivos adicionales para la terapia génica de la enfermedad de Batten CLN6…(inglés)
- Elsevier Inc. La terapia génica corrige patologías cerebrales y conductuales en la enfermedad de CLN6-Batten.. (inglés)
- Batten Disease. Viviendo con la enfermedad de Batten (inglés)
- Joana Carvalho. Una sustáncia química podría ayudar a los afectados por la enfermedad de Batten a prevenir la muerte celular. (inglés)
- Batten Disease News. Scientist Wins Grant to Study CLN6 Batten, Advance Early Trials – Batten Disease News
- Europapress. Investigador de la USAL avanza en identificación de nuevos mecanismos neurodegenerativos en la enfermedad de Batten (europapress.es)
- Beyond Batten Disease Foundation. Investigación de tratamiento con Batten-1 (basado en Miglustat) para enfermedad de Batten CLN3
Referencias científicas revisadas y recomendadas
- Lopez-Fabuel I, Garcia-Macia M, Buondelmonte C, Burmistrova O, Bonora N, Alonso-Batan P, Morant-Ferrando B, Vicente-Gutierrez C, Jimenez-Blasco D, Quintana-Cabrera R, Fernandez E, Llop J, Ramos-Cabrer P, Sharaireh A, Guevara-Ferrer M, Fitzpatrick L, Thompton CD, McKay TR, Storch S, Medina DL, Mole SE, Fedichev PO, Almeida A, Bolaños JP. Aberrant upregulation of the glycolytic enzyme PFKFB3 in CLN7 neuronal ceroid lipofuscinosis. Nat Commun. 2022 Jan 27;13(1):536. doi: 10.1038/s41467-022-28191-1. PMID: 35087090
En este artículo original (en inglés), los investigadores principales, de la Universidad de Salamanca, han encontrado en un modelo de ratón CLN7, un fallo en la autofagia (sistema de limpieza de desechos en las células) que produce un acúmulo de mitocondrias alteradas. Esto produce un aumento de radicales libres en las mitocondrias que está mediado por una enzima, la PFKFB3, que se activa cuando no debería. Estos investigadores aplican un bloqueador de PFKFB3 llamado AZ67 a las células afectadas y éstas mejoran, desapareciendo la situación de estrés en las células CLN7. Concluyen que diseñar terapias dirigidas a la enzima PFKFB3 podría ser una nueva línea terapéutica en enfermedades lisosomales.
- Specchio N, Ferretti A, Trivisano M, Pietrafusa N, Pepi C, Calabrese C, Livadiotti S, Simonetti A, Rossi P, Curatolo P, Vigevano F. Neuronal Ceroid Lipofuscinosis: Potential for Targeted Therapy. Drugs. 2021 Jan;81(1):101-123. doi: 10.1007/s40265-020-01440-7. PMID: 33242182.
En este artículo de revisión (inglés), los autores del Hospital Bambino Gesú de Roma, especialistas en epilepsia y enfermedades neurogenéticas, hacen una revisión de las líneas terapéuticas disponibles en la actualidad para cada tipo de NCL.
- Mole SE, Cotman SL. Genetics of the neuronal ceroid lipofuscinoses (Batten disease). Biochim Biophys Acta. 2015 Oct;1852(10 Pt B):2237-41. doi: 10.1016/j.bbadis.2015.05.011. PMID: 26026925.
En este artículo de revision (inglés), los autores, del University College de Londres, hacen una actualización sobre la genética de la NCL y las posibles correlaciones genotipo-fenotipo. Es decir, si existe una asociación entre una mutación concreta y la aparición más temprana o tardía de síntomas, o que estos síntomas sean más leves o severos.